O ensaio clínico
Podense atopar tantas definicións de ensaio clínico como enfoques posibles ten o tema, aínda que predomina o enfoque epidemiolóxico e o finalista (o seu uso para investigar fármacos). Podemos dicir que o ensaio clínico consiste nun estudo experimental e prospectivo no cal o investigador provoca e controla as variables e os suxeitos (pacientes, a maioría dos casos) son asignados de forma aleatoria ás distintas intervencións que se comparan.
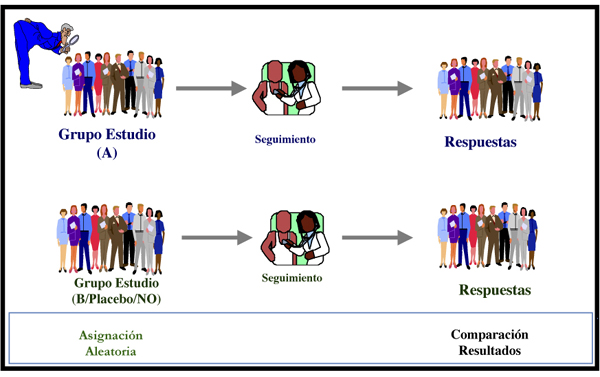
O elemento esencial do ensaio é a existencia dun grupo de comparación ou grupo de control, que permite probar se a nova intervención (por exemplo un novo fármaco) é mellor ou non que as xa existentes ou que non intervir (placebo).
Un ensaio clínico iníciase cando xorde unha hipótese a partir de estudos non controlados observacionales, descritivos ou retrospectivos, ou de estudos preclínicos. Frecuentemente descóbrense en investigacións preclínicas posibilidades terapéuticas que non teñen ningún beneficio nun ensaio clínico. Despois de ser deseñado debe ser aprobado por un comité de bioética, os pacientes que forman parte deben coñecer os obxectivos do estudo, os seus riscos e beneficios e asinar o consentimento informado e poderán abandonar o estudo cando queiran. O ensaio clínico finaliza cando acaban os prazos de tempo definidos no protocolo, ou cando de forma prematura son manifestamente prexudiciais ou beneficiosos os efectos no brazo experimental.
Como se realiza un ensaio clínico?
- Investigación básica. Antes de poder iniciar un ensaio clínico, os médicos deben ter algunha teoría sobre o motivo polo cal un tratamento novo podería ser eficaz. En xeral, formular unha teoría require moitos anos de investigación.
- Estudos en animais. Os médicos proban primeiro o tratamento novo en animais para determinar se podería ser beneficioso ou prexudicial para as persoas.
- A proposta. Unha vez que os médicos que realizan o estudo demostran que o novo tratamento é inocuo en animais, preséntase unha proposta a un grupo de médicos, estatísticos, científicos e individuos da comunidade que son membros dunha xunta de revisión institucional (JRI) independente
- Procura de pacientes. Tras recibir a aprobación da JRI, os médicos deben atopar pacientes para o estudo. Todos os pacientes que participan nun ensaio clínico son voluntarios.
- Consentimento informado. Antes de que os pacientes poidan participar nun ensaio clínico deben asinar un formulario de consentimento informado. Este formulario informa os pacientes sobre os riscos e beneficios do estudo, para que poidan decidir se desexan participar.
O ensaio clínico esta dividido en catro fases:
- Primeira fase. Esta parte do ensaio clínico tamén se denomina «estudo de inocuidad». Conta coa participación de relativamente poucos pacientes e dura ao redor dun ano. A primeira fase determina se o estudo é inocuo e se debe continuarse nun grupo máis grande de persoas.-
- Segunda fase. Esta parte do ensaio clínico conta coa participación dun número máis grande de pacientes. Este é o momento en que os médicos elixen un grupo de persoas que será o grupo de control. O grupo de control recibirá o mellor tratamento dispoñible ou un placebo (ningún tratamento). Na maioría dos ensaios clínicos, é raro que os pacientes que integran o grupo de control non reciban tratamento algún. En cambio, xeralmente reciben o mellor tratamento dispoñible. A segunda fase pode durar moitos anos.
- Terceira fase. Este é o último paso antes de que se aprobe o tratamento. A terceira fase pode contar coa participación de miles de pacientes e durar tanto como cinco anos. Durante esta fase, compárase aos pacientes que reciben o tratamento novo con aqueles que recibiron outros tratamentos ou un placebo.
- Cuarta fase (aprobación). Se os médicos determinan que o novo tratamento é eficaz, a Administración de Drogas e Alimentos dos Estados Unidos (FDA) aprobarao para uso xeral. Mesmo despois de obtida a aprobación, séguese vixiando o tratamento. Todo problema debe ser comunicado á FDA durante os 10 anos seguintes á aprobación
Na miña opinión os ensaios clínicos son unha boa maneira de probar os medicamentos ou os diferentes métodos de cura antes de espoñelos ante todo o mudo, xa que, desta maneira si un medicamento tivera un efecto secundario grave non afectaría a todos os consumidores desa menciña e polo tanto no sairía ao mercado.
Fontes:
Wikipedia. Enciclopedia virtual : http://es.wikipedia.org/wiki/Ensayo_cl%C3%ADnico
Texas Heart Institute:Texas: http://www.texasheart.org/HIC/Topics_Esp/FAQ/clinical_trials_span.cfm
Esta entrada foi elaborada no curso 2014-15 por Christopher Vázquez
Tags: Bioética, efecto placebo
